Hidrokarbon Kelas 11 Kurikulum 2013 - pengertian, tata nama, contoh
Pengertian dan klasifikasi Hidrokarbon
Hidrokarbon adalah golongan senyawa karbon yang paling sederhana, yaitu istilah mengacu pada senyawa yang tersusun dari atom karbon dan hidrogen. Hidrokarbon dan senyawa turunannya terbagi menjadi tiga kelompok besar pada umumnya, yaitu :
Propana Pentana

Pengertian dan Kekhasan Atom Karbon
Senyawa karbon adalah semua senyawa yang mengandung rantai karbon. Senyawa karbon disebut juga senyawa organik, karena dahulu ada anggapan bahwa senyawa organik berasal dari bahan kehidupan baik hewan maupun tumbuhan. Kimia organik merupakan salah satu cabang kimia yang mempelajari senyawa organik atau senyawa karbon.
1. Atom karbon dengan nomor atom 6 dan mempunyai konfigurasi elektron 2, 4. Karbon dapat berikatan kovalen dengan mengunakan keempat elektron valensinya.
2. Atom karbon relatif kecil, hal ini sesuai dengan periodenya yaitu periode 2 sehingga hanya mempunyai dua kulit atom yang menyebabkan jari – jari atom relatif kecil. Dengan relatif kecilnya jari-jari atom, atom karbon mempunyai dua keuntungan :
(1) Ikatan kovalen yang dibentuk karbon relatif kuat.
(2) Karbon dapat membentuk ikatan rangkap dua dan ikatan rangkap tiga.
3. Atom karbon mempunyai kemampuan untuk ikatan rantai.
Atom karbon dapat mengikat atom karbon lain terbentuklah ikatan rantai atom karbon. Ikatan rantai atom karbon dapat berupa :
Contoh :
C – C – C – C
|
C - C - C - C
|
C
4. Ikatan antara atom – atom C dapat secara :
C ― C
Senyawa karbon yang memiliki ikatan rangkap disebut senyawa tak jenuh.
5. Berdasarkan jumlah atom karbon yang diikatnya, posisi atom karbon dibedakan :
Contoh :
C7 C8
| |
C1 — C2 — C3 — C4 — C5 — C6
|
C9
Atom C primer adalah = 1, 6, 7, 8, 9.
Atom C sekunder adalah = 3, 5
Atom C tersier adalah = 2
Atom C kwarter adalah = 4
Tata nama senyawa Hidrokarbon
1. Alkana ( Rangkap Tunggal )
Alkana merupakan hidrokarbon alifatik jenuh yang masing – masing atom karbonnya terikat pada keempat atom lain.
Alkana disebut juga parafin ( miskin daya reaksi ) dengan rumus umum CnH2n+2. Suatu kelompok senyawa karbon dengan rumus yang sama dan kemiripan sifatnya besar disebut satu homolog ( deret sepancaran ). Contoh – contoh alkana dapat dilihat pada tabel berikut :
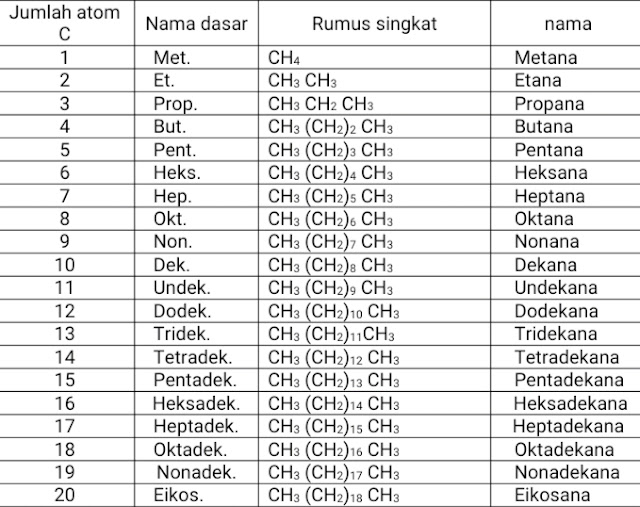
A. Tata Nama Alkana
Para kimiawan sesungguhnya menggunakan banyak sistem tata nama yang berbeda – beda, disini akan diberikan cara yang bersistem dari tata nama IUPAC ( International Union of Pureaud Applied Chemistry ) yaitu Persatuan Kimia Murni dan Terapan Internasional, karena cara ini memberikan pendekatan yang lebih tepat dalam memberikan nama dan menggambarkan senyawa organik.
Nama induk diturunkan dari kata dasar, biasanya dari kata Yunani yang menunjukan jumlah atom karbon dalam rangkaian rantai atom C. Kemudian akhiran –ana diimbuhkan pada kata dasar untuk melengkapi nama induk suatu alkana. Nama suatu alkana normal sesuai dengan nama induknya.
Contoh :
CH3(CH2)6CH3
Contoh :
CH3
|
1 2 3
CH3 — CH — C — CH3
| |
CH3 4 5
CH2 — CH3
Rangkaian atom C dinomori adalah rantai induk.
2. menuliskan nomor atom C utama ( induk )di mulai dari ujung, jika :
5 4 3 2 1
CH3 — CH2 — CH3 — CH2 — CH3
|
CH3
Ujung kiri omor 2 merupakan rantai yang terdapat cabangnya, sehingga penomoran dimulai dari kiri
3. menuliskan nomor C yang ditempati cabang, diikuti nama cabang kemudian dituliskan nama rantai induk / utamanya.
Pada rantai cabang untuk diperhatikan :
CH3 yang terangkai pada rantai induk disebut metil.
CH2CH3 disebut etil dan seterusnya.
1. CH3
|
1 2 3 4 5 6
CH3 — CH — CH2 — CH2 — CH2 — CH3
2 - metilheksana
2. CH3
|
1 2 3 4
CH3 — C — CH2 — CH3
|
CH3
2, 2 - dimetilbutana
C. Sumber dan Kegunaan Alkana
a. Bahan bakar, misalnya LPG, minyak tanah, bensin dan solar.
b. Sebagai bahan pelarut dalam industri, misalnya petroleum eter, dan nafta.
c. Sebagai sumber gas hidrogen.
d. Sebagai pelumas, misalnya vaselin dan oil.
e. Sebagai bahan baku industri, misalnya minyak bumi sebagai bahan pembuatan plastik, detergen, karet sintetis, serat sintetis, minyak rambut, dan obat gosok.
2. Alkena ( Rangkap Dua )
Alkena merupakan hidrokarbon yang memiliki satu ikatan rangkap dua karbon – karbon. Senyawa ini dikatakan tidak jenuh karena tidak mempunyai jumlah maksimum atom yang sebetulnya dapat ditampung oleh setiap atom karbon. Alkena disebut juga olefin karena dari kenyataan klor mengadisi etilena yang berbentuk gas ( C2H4 ) membentuk hasil yang menyerupai minyak. Alkena mempunyai rumus umum CnH2n, berikut akan diberikan contoh – contoh alkena.

A. Tata Nama Alkena
Contoh :
CH2— CH3
|
1 2 3 4 5 6
CH2 = CH — CH — CH2— CH2— CH3
Rangkaian atom C yang dinomori merupakan rantai induk
(2) Menuliskan nomor atom C utama ( induk ) dan nomor ikatan rangkap, dimulai dari ujung, ujung paling dekat dengan ikatan rangkapnya.
Contoh :
1 1 2 2 3 4 5
CH3 — CH = CH — CH2 — CH3
Karena ujung kiri lebih dekat dengan rangkap ( no 2 biru ), maka penomoran dilakukan dari ujung kiri
5 4 3 2 2 1 1
CH3 — CH — CH = CH — CH3
|
CH3
Karena ujung kanan lebih dekat dengan rangkap ( no 1 biru ), maka penomoran delakukan dari ujung kanan
(3) Menuliskan unsur C utama yang ditempati cabang dikuti nama cabang, kemudian dituliskan nomor ikatan rangkapnya dan kemudian dituliskan nama rantai induk alkenanya.
Contoh Soal :
1.
1 1 2 2 3 4
CH3 —CH = CH — CH3
2 - butena
2. CH3
|
7 6 5 4 3 3 2 2 1 1
CH3 — CH2 — CH — CH = CH — CH2 — CH3
5 - metil - 3 - heptena
B. Sumber dan Kegunaan Alkena
Dalam industri alkena di buat dari alkana dengan proses Cracking (perengkahan). Alkena suhu rendah merupakan bahan baku yang sangat penting dalam industri untuk pembuatan plastik, karet sintetis dan alkohol.
3. Alkuna ( Rangkap Tiga )
Alkuna adalah hidrokarbon tak jenuh yang memiliki satu ikatan rangkap tiga karbon – karbon. Alkuna yang paling sederhana adalah Asetelina / etuna ( C2H2 ), yang merupakan gas penting. Alkuna sering disebut Asetilena dengan rumus umum CnH2n-2, berikut akan diberikan contoh – contoh senyawa alkuna.

A. Tata Nama Alkuna
B. Sumber dan Kegunaan Alkuna
Diantara golongan alkuna yang mempunyai nilai ekonomis hanyalah etuna / asetilen ( C2H2 ). Dalam jumlah sedikit C2H2 dibuat dari reaksi batu karbit ( kalsium karbida ) dengan air.
CaC2 + 2H2O — Ca(OH)2 + C2H2
Dalam jumlah besar ( industri ), C2H2 dibuat melalui pembakaran tidak sempurna dari metana.
4CH4 + 3O2 — 2C2H2 + 6H2O
Gas asitilen ( etuna ) dimanfaatkan dalam industri pemotongan / -penyambungan baja.
Rangkuman
Hidrokarbon adalah golongan senyawa karbon yang paling sederhana, yaitu istilah mengacu pada senyawa yang tersusun dari atom karbon dan hidrogen. Hidrokarbon dan senyawa turunannya terbagi menjadi tiga kelompok besar pada umumnya, yaitu :
- Hidrokarbon alifatik terdiri atas rantai terbuka atau hidrokarbon asiklik
Propana Pentana
- Hidrokarbon alisiklik atau hidrokarbon siklik terdiri atas atom karbon yang tersusun dalam satu lingkar atau lebih. Contoh : Siklo propana dan Siklo pentana
- Hidrokarbon aromatik adalah golongan khusus senyawa siklik yang digambarkan sebagai lingkar enam dengan ikatan selang – seling antara tunggal dan rangkap. Kelompok ini digolongkan terpisah dari hidrokarbon alisiklik dan alifalik karena sifat fisika dan kimianya yang khas. Contoh : Benzena dan Naftalena

Sebelum lanjut Sobat harus mengetahui apa itu senyawa karbon dan apa yang menjadi ciri khas senyawa karbon. Hal ini dimaksudkan untuk lebih mudah memahami materi selanjutnya, ringlasannya yaitu :
Senyawa karbon adalah semua senyawa yang mengandung rantai karbon. Senyawa karbon disebut juga senyawa organik, karena dahulu ada anggapan bahwa senyawa organik berasal dari bahan kehidupan baik hewan maupun tumbuhan. Kimia organik merupakan salah satu cabang kimia yang mempelajari senyawa organik atau senyawa karbon.
1. Atom karbon dengan nomor atom 6 dan mempunyai konfigurasi elektron 2, 4. Karbon dapat berikatan kovalen dengan mengunakan keempat elektron valensinya.
|
― C ―
|
Tiap garis menyatakan satu elektron valensi atau satu ikatan kovalen.
2. Atom karbon relatif kecil, hal ini sesuai dengan periodenya yaitu periode 2 sehingga hanya mempunyai dua kulit atom yang menyebabkan jari – jari atom relatif kecil. Dengan relatif kecilnya jari-jari atom, atom karbon mempunyai dua keuntungan :
(1) Ikatan kovalen yang dibentuk karbon relatif kuat.
(2) Karbon dapat membentuk ikatan rangkap dua dan ikatan rangkap tiga.
3. Atom karbon mempunyai kemampuan untuk ikatan rantai.
Atom karbon dapat mengikat atom karbon lain terbentuklah ikatan rantai atom karbon. Ikatan rantai atom karbon dapat berupa :
- Rantai C terbuka
Contoh :
C – C – C – C
- Rantai C tertutup ( lingkar )
- Rantai C bercabang
|
C - C - C - C
|
C
4. Ikatan antara atom – atom C dapat secara :
- Ikatan tunggal
C ― C
- Ikatan rangkap
Senyawa karbon yang memiliki ikatan rangkap disebut senyawa tak jenuh.
5. Berdasarkan jumlah atom karbon yang diikatnya, posisi atom karbon dibedakan :
- Atom C primer yaitu satu atom C mengikat 1 atom C yang lain.
- Atom C sekunder yaitu satu atom C mengikat 2 atom C yang lain.
- Atom C tersier yaitu satu atom C mengikat 3 atom C yang lain.
- Atom C kwarter yaitu satu atom C mengikat 4 atom C yang lain.
Contoh :
C7 C8
| |
C1 — C2 — C3 — C4 — C5 — C6
|
C9
Atom C primer adalah = 1, 6, 7, 8, 9.
Atom C sekunder adalah = 3, 5
Atom C tersier adalah = 2
Atom C kwarter adalah = 4
Tata nama senyawa Hidrokarbon
1. Alkana ( Rangkap Tunggal )
Alkana merupakan hidrokarbon alifatik jenuh yang masing – masing atom karbonnya terikat pada keempat atom lain.
Alkana disebut juga parafin ( miskin daya reaksi ) dengan rumus umum CnH2n+2. Suatu kelompok senyawa karbon dengan rumus yang sama dan kemiripan sifatnya besar disebut satu homolog ( deret sepancaran ). Contoh – contoh alkana dapat dilihat pada tabel berikut :

A. Tata Nama Alkana
Para kimiawan sesungguhnya menggunakan banyak sistem tata nama yang berbeda – beda, disini akan diberikan cara yang bersistem dari tata nama IUPAC ( International Union of Pureaud Applied Chemistry ) yaitu Persatuan Kimia Murni dan Terapan Internasional, karena cara ini memberikan pendekatan yang lebih tepat dalam memberikan nama dan menggambarkan senyawa organik.
- Untuk nama alkana normal ( tidak bercabang ).
Nama induk diturunkan dari kata dasar, biasanya dari kata Yunani yang menunjukan jumlah atom karbon dalam rangkaian rantai atom C. Kemudian akhiran –ana diimbuhkan pada kata dasar untuk melengkapi nama induk suatu alkana. Nama suatu alkana normal sesuai dengan nama induknya.
Contoh :
CH3(CH2)6CH3
Kata dasarnya adalah okt. ( karena ada 8 atom C )
kemudian diimbuhkan –ana, sehingga mempunyai nama oktana.
- Untuk nama alkana bercabang.
Contoh :
CH3
|
1 2 3
CH3 — CH — C — CH3
| |
CH3 4 5
CH2 — CH3
Rangkaian atom C dinomori adalah rantai induk.
2. menuliskan nomor atom C utama ( induk )di mulai dari ujung, jika :
- Ujung paling dekat dengan cabang
- Jika terdapat dua ujung yang keduanya berdekatan dengan cabang, maka pilih yang lebih panjang cabangnya
5 4 3 2 1
CH3 — CH2 — CH3 — CH2 — CH3
|
CH3
Ujung kiri omor 2 merupakan rantai yang terdapat cabangnya, sehingga penomoran dimulai dari kiri
3. menuliskan nomor C yang ditempati cabang, diikuti nama cabang kemudian dituliskan nama rantai induk / utamanya.
Pada rantai cabang untuk diperhatikan :
- Rantai cabang hidrokarbon diberi nama dengan menggunakan nama dasar yang tepat yang diberi nama akhiran – il.
CH3 yang terangkai pada rantai induk disebut metil.
CH2CH3 disebut etil dan seterusnya.
- Rantai cabang ganda diberi nama dengan awalan bilangan yunani yang sesuai yaitu di- untuk dua, tri- untuk tiga, dan seterusnya.
- Apabila dua atau lebih rantai cabang yang berbeda di rangkaikan pada rantai induknya, nama dari rantai itu disusun menurut abjad di dalam senyawanya.
1. CH3
|
1 2 3 4 5 6
CH3 — CH — CH2 — CH2 — CH2 — CH3
2 - metilheksana
2. CH3
|
1 2 3 4
CH3 — C — CH2 — CH3
|
CH3
2, 2 - dimetilbutana
C. Sumber dan Kegunaan Alkana
- Sumber Alkana
- Kegunaan Alkana
a. Bahan bakar, misalnya LPG, minyak tanah, bensin dan solar.
b. Sebagai bahan pelarut dalam industri, misalnya petroleum eter, dan nafta.
c. Sebagai sumber gas hidrogen.
d. Sebagai pelumas, misalnya vaselin dan oil.
e. Sebagai bahan baku industri, misalnya minyak bumi sebagai bahan pembuatan plastik, detergen, karet sintetis, serat sintetis, minyak rambut, dan obat gosok.
2. Alkena ( Rangkap Dua )
Alkena merupakan hidrokarbon yang memiliki satu ikatan rangkap dua karbon – karbon. Senyawa ini dikatakan tidak jenuh karena tidak mempunyai jumlah maksimum atom yang sebetulnya dapat ditampung oleh setiap atom karbon. Alkena disebut juga olefin karena dari kenyataan klor mengadisi etilena yang berbentuk gas ( C2H4 ) membentuk hasil yang menyerupai minyak. Alkena mempunyai rumus umum CnH2n, berikut akan diberikan contoh – contoh alkena.

A. Tata Nama Alkena
- Untuk alkena normal mengikuti aturan yang serupa dengan aturan alkana, kemudian mengganti akhiran ana menjadi ena.
- Untuk alkena bercabang :
Contoh :
CH2— CH3
|
1 2 3 4 5 6
CH2 = CH — CH — CH2— CH2— CH3
Rangkaian atom C yang dinomori merupakan rantai induk
(2) Menuliskan nomor atom C utama ( induk ) dan nomor ikatan rangkap, dimulai dari ujung, ujung paling dekat dengan ikatan rangkapnya.
Contoh :
1 1 2 2 3 4 5
CH3 — CH = CH — CH2 — CH3
Karena ujung kiri lebih dekat dengan rangkap ( no 2 biru ), maka penomoran dilakukan dari ujung kiri
5 4 3 2 2 1 1
CH3 — CH — CH = CH — CH3
|
CH3
Karena ujung kanan lebih dekat dengan rangkap ( no 1 biru ), maka penomoran delakukan dari ujung kanan
(3) Menuliskan unsur C utama yang ditempati cabang dikuti nama cabang, kemudian dituliskan nomor ikatan rangkapnya dan kemudian dituliskan nama rantai induk alkenanya.
Contoh Soal :
1.
1 1 2 2 3 4
CH3 —CH = CH — CH3
2 - butena
2. CH3
|
7 6 5 4 3 3 2 2 1 1
CH3 — CH2 — CH — CH = CH — CH2 — CH3
5 - metil - 3 - heptena
B. Sumber dan Kegunaan Alkena
Dalam industri alkena di buat dari alkana dengan proses Cracking (perengkahan). Alkena suhu rendah merupakan bahan baku yang sangat penting dalam industri untuk pembuatan plastik, karet sintetis dan alkohol.
3. Alkuna ( Rangkap Tiga )
Alkuna adalah hidrokarbon tak jenuh yang memiliki satu ikatan rangkap tiga karbon – karbon. Alkuna yang paling sederhana adalah Asetelina / etuna ( C2H2 ), yang merupakan gas penting. Alkuna sering disebut Asetilena dengan rumus umum CnH2n-2, berikut akan diberikan contoh – contoh senyawa alkuna.

A. Tata Nama Alkuna
- Untuk alkuna normal diturunkan dari alkana yang sesuai, kemudian mengganti ana menjadi una.
- Untuk alkuna bercabang.
B. Sumber dan Kegunaan Alkuna
Diantara golongan alkuna yang mempunyai nilai ekonomis hanyalah etuna / asetilen ( C2H2 ). Dalam jumlah sedikit C2H2 dibuat dari reaksi batu karbit ( kalsium karbida ) dengan air.
CaC2 + 2H2O — Ca(OH)2 + C2H2
Dalam jumlah besar ( industri ), C2H2 dibuat melalui pembakaran tidak sempurna dari metana.
4CH4 + 3O2 — 2C2H2 + 6H2O
Gas asitilen ( etuna ) dimanfaatkan dalam industri pemotongan / -penyambungan baja.
Rangkuman
- Senyawa karbon adalah senyawa yang mengandung unsur karbon.
- Senyawa karbon juga mengandung unsur hidrogen, oksigen, nitrogen, belerang, dan fosfor.
- Sumber senyawa karbon adalah mahluk hidup dan sisa – sisa mahluk hidup.
- Berdasarkan proses terbentuknya senyawa karbon dibedakan menjadi senyawa karbon organik dan senyawa karbon anorganik.
- Senyawa karbon organik memegang peranan penting dalam kimia yang berasal dari mahluk hidup.
- Keunikan atom karbon karena mempunyai empat elektron valensi dan jari – jari atom yang tegolong kecil.
- Senyawa hidrokarbon terdiri atas karbon dan hidrogen. Metana merupakan hidrokabon paling sederhana.
- Atom karbon mempunyai kemampuan membentuk empat ikatan kovalen. Atom karbon mempunyai kemampuan membentuk rantai.
- Berdasarkan bentuk rantainya, hidrokarbon dapar dibagi kedalam senyawa alifatik, alisiklik dan aromatik.
- Alkana mempunayi rumus umum CnH2n + 2. Senyawa ini disebut juga hidrokarbon jenuh tergolong dalam senyawa alifatik. Senyawa ini menunjukkan peristiwa keisomeran.
- Alkena mengandung satu ikatan rangkap dua dan mempunyai rumus umum CnH2n, disebut juga hidrokarbon tak jenuh.
- Alkuna mengandung satu ikatan rangkap tiga dan mempunyai rumus umum CnH2n – 2, tergolong hidrokarbon tak jenuh.
- Alkana adalah senyawa yang kurang reaktif sehingga disebut parafin. Reaksi penting alkana adalah pembakaran, substitusi, dan perengkahan.
- Alkena dan alkuna lebih reaktif daripada alkana karena mengandung ikatan rangkap dua dan rangkap tiga.
- Sumber utama alkana adalah minyak bumi dan gas alam.
- Alkena dibuat dari alkana dengan proses cracking, sedang alkuna dibuat dari gas alam dan reaksi batu karbit dengan air.
Belum ada Komentar untuk "Hidrokarbon Kelas 11 Kurikulum 2013 - pengertian, tata nama, contoh"
Posting Komentar